Čeští vědci přišli na příčinu rozvoje onemocnění zvaného AA amyloidóza u některých pacientů. Jde o genetický přenos mutace v genu SAA1. Ten zvyšuje produkci bílkoviny v těle a vede k selhání ledvin.
Vědci již navrhli i účinnou léčbu… AA amyloidóza je závažné, byť ne příliš časté onemocnění, jež u pacientů končívá selháním ledvin. U více než poloviny pacientů vzniká v důsledku chronického zánětu nebo infekce v organismu.
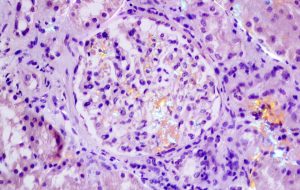 „AA amyloidóza je nemoc, při které v důsledku dlouhodobého zánětu dochází k nadměrné produkci specifické bílkoviny – sérového amyloidního A proteinu [SAA1]. Bílkovina se následně shlukuje a ukládá v různých orgánech těla a zhoršuje jejich funkci,“ vysvětluje jeden z hlavních autorů výzkumu Jakub Sikora z Laboratoře pro studium vzácných nemocí Kliniky pediatrie a dědičných poruch metabolismu 1. LF UK a Všeobecné fakultní nemocnice [VFN].
„AA amyloidóza je nemoc, při které v důsledku dlouhodobého zánětu dochází k nadměrné produkci specifické bílkoviny – sérového amyloidního A proteinu [SAA1]. Bílkovina se následně shlukuje a ukládá v různých orgánech těla a zhoršuje jejich funkci,“ vysvětluje jeden z hlavních autorů výzkumu Jakub Sikora z Laboratoře pro studium vzácných nemocí Kliniky pediatrie a dědičných poruch metabolismu 1. LF UK a Všeobecné fakultní nemocnice [VFN].
Podle něj jsou onemocněním nejčastěji postiženy ledviny. Léčba pacientů s AA amyloidózou dosud spočívá výhradně v kompenzaci jejich základního onemocnění [Na fotografii výše: Tkáň ledviny postižená ukládáním amyloidu – zeleno-oranžové oblasti, zdroj: 1. LF UK].
Až u 20 % pacientů lékaři neznají příčinu onemocnění
Lékaři v posledních letech sledují trend, jak mezi pacienty s AA amyloidózou roste podíl nemocných bez zjevné základní příčiny onemocnění. Tito pacienti netrpí žádnou chronickou zánětlivou či infekční nemocí. A pacienty bez základní diagnózy nemají, jak léčit. Jde přitom o život ohrožující onemocnění. To, když je neléčené, vede k chronickému selhání ledvin, nedostatečné výživě, závislosti na dialýze, k opakovaným transplantacím ledvin i úmrtí.
„Spekulovalo se, že u některých z těchto pacientů by AA amyloidóza mohla být dědičná a vznikat v důsledku mutací přímo v genu SAA1. Pro tuto domněnku ale nebyly žádné důkazy,“ říká Sikora.
Počátky výzkumu příčin vzniku onemocnění u těchto pacientů nastal v roce 2006, kdy vědce z tehdejšího Ústavu dědičných metabolických poruch oslovila profesorka Zdeňka Vernerová z Ústavu patologie 3. LF UK a Fakultní nemocnice Královské Vinohrady. Tehdy jim předložila nález AA amyloidózy u jedné ze svých pacientek, jejíž vzorky ledvin a štítné žlázy vyšetřovala.
„Základní klinická příčina vysvětlující ukládání SAA1 u nemocné, ale chyběla. Podobné onemocnění u dalších pacientčiných příbuzných vyvolávalo podezření z dědičné povahy amyloidózy v rodině,“ popisuje začátky výzkumu, který nakonec trval 16 let, Jakub Sikora.
16 let pátrání po genetické příčině onemocnění
Podle Sikory tehdy začalo mnohaleté, takřka detektivní pátrání po dalších členech rodiny zmiňované pacientky. A to ať už žijících i zemřelých. Vědci hledali jejich společné genetické mutace, které by mohly nadprodukci bílkoviny způsobovat. Dohledávali staré pitevní protokoly a tkáňové vzorky zemřelých příbuzných. Žijící členy rodiny z různých částí republiky se postupně podařilo svolat na Kliniku nefrologie 1. LF UK a VFN, kde je pak začala klinicky sledovat a léčit profesorka Romana Ryšavá.
„Pacientům jsme zkoušeli nejprve nasadit nespecifickou léčbu, která u řady nemocných s amyloidózou může zmírnit projevy onemocnění, dále kortikosteroidy a v některých případech i imunosupresiva,“ popisuje profesorka Ryšavá.
Nic z toho ale nevedlo ke snížení produkce bílkoviny a omezení projevů nemoci. Navíc nasazovaná léčba byla podle ní spojena s nepřiměřenou toxicitou. Lékaři tak po dobu 16 let monitorovali čtyři generace několika větví rodiny. Někteří z jejích členů v průběhu času na onemocnění zemřeli, u dalších došlo k postupnému rozvoji AA amyloidózy.
Vědci nakonec objevili mutaci zvyšující produkci bílkoviny
Po 16 letech klinického sledování všech členů rodiny, kdy vědečtí pracovníci pečlivě analyzovali odebrané tkáně, proteiny a nakonec i celogenomově sekvenovali vzorky všech pacientů v rodině, se podařilo zjistit sdílenou příčinnou mutaci v genu SAA1 [ten zvyšuje produkci bílkoviny, pozn. red.].
„Našli jsme tak jako první na světě rodinu, ve které se AA amyloidóza dědí na podkladě mutace přímo v genu SAA1,“ zdůrazňuje Jakub Sikora.
Upozorňuje, že pro tyto pacienty, respektive pacienty s takto dědičnou AA amyloidózou může existovat i účinná léčba. Profesorka Ryšavá jim zprvu experimentálně nasadila monoklonální protilátku tocilizumab. Jde o lék, kterým se v současnosti mimo jiné léčí i onemocnění covid-19. Lék blokuje imunitní reakce.
„Jelikož víme, že ve vzniku AA amyloidózy hrají klíčovou roli dva cytokiny – interleukin 1 a interleukin 6 – bylo logickou volbou zkusit zablokovat signalizaci některým z nich, a tím se pokusit onemocnění ovlivnit,“ vysvětluje profesorka Ryšavá.
Podle ní už první pacientka lék velmi dobře tolerovala. A její zdravotní stav se podle ní i poměrně rychle zlepšil. Dále tvrdí, že nová zjištění o příčině vzniku onemocnění AA amyloidóza u pacientů, u nichž nejsou lékaři schopni odhalit základní příčinu onemocnění, povedou k rychlejší diagnostice. Podle jejích odhadů by dnes mohlo jít zhruba o 15 až 20 procent všech pacientů s AA amyloidózou. Správná molekulární diagnóza u nich totiž pomůže zahájit léčbu dříve, než dojde k masivnímu ukládání bílkoviny do tkání.
„Podávání tocilizumabu je částečně efektivní, ideální by ale bylo zahájit vývoj léků cílených přímo na SAA1 či jiné [dosud neidentifikované] mutované geny na bázi monoklonálních protilátek či malých interferujících RNA,“ říká profesorka Ryšavá.
Do projektu byli v jeho posledních fázích přizváni také experti z Mayo Clinic a Wake Forest School of Medicine v USA. Význam průlomového objevu českých vědců dokládá i to, že jeho výsledky publikoval prestižní časopis Kidney International.
–VRN–