Evropská agentura pro léčivé přípravky [EMA] doporučila Evropské komisi schválit lék Voxzogo [účinná látka vosoritid] k léčbě achondroplázie. Lidé s touto nemocí jsou malého vzrůstu, průměrně dorůstají do výšky okolo 130 cm.
Ještě před evropským regulátorem lék koncem loňského roku schválil americký Úřad pro kontrolu potravin a léčiv [FDA]. Účinná látka vosoritid na achondroplázii, kterou vyvinula americká firma BioMarin Pharmaceutical, je testována déle než šest let.
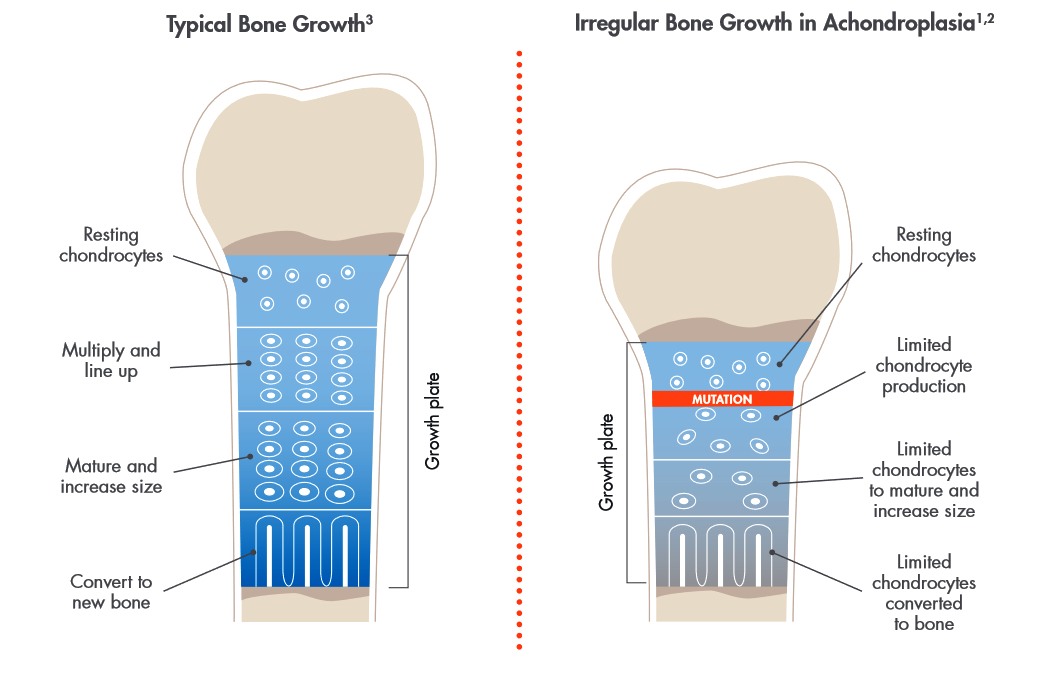
Achondroplázie je nejčastější forma genetické poruchy růstu a vývoje kostry u člověka, která je způsobena mutacemi v genu pro růstový faktor FGFR3. Zjednodušeně řečeno jde o selhání normální přeměny chrupavky na kost, což brání růstu kostí. Lidé trpící touto nemocí mají krátké dolní a horní končetiny při normální velikosti trupu [Ilustrace: BioMarin Pharmaceutical].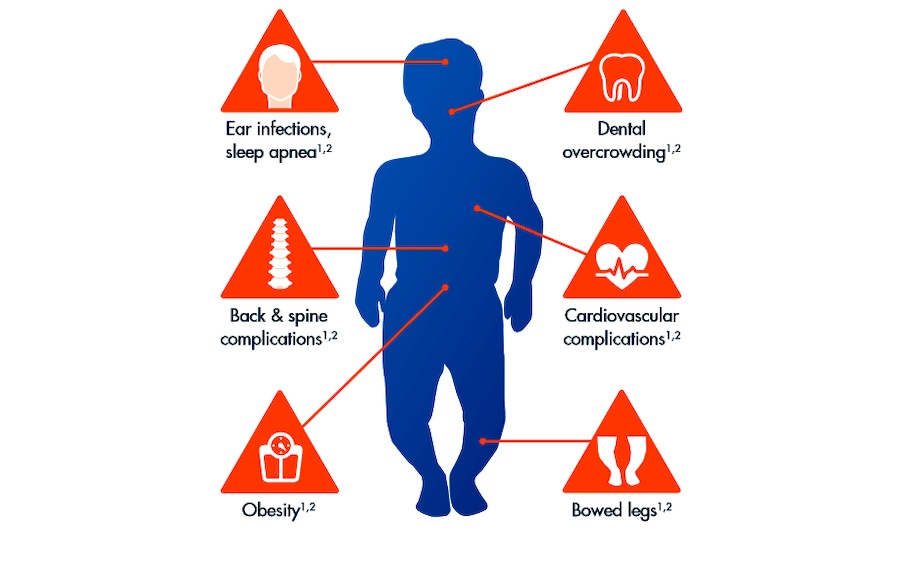
Podle odhadů se v EU každý rok narodí 350 dětí s achondroplázií. Z toho v Česku pak čtyři až pět dětí s touto poruchou růstu. Komplexní léčba achondroplázie zatím neexistuje.
Vosoritid tlumí aktivitu FGFR3
EMA doporučila využívat léčivý přípravek u pacientů starších dvou let. Před zahájením léčby musí dítě projít podrobným genetickým vyšetřením. U pacientů s achondroplázií je gen fibroblastového receptoru pro růstový faktor 3 [FGFR3] stále „zapnutý“ a brání normálnímu růstu kostí.
Účinná látka vosoritid působí tak, že se na povrchu buněk naváže na receptor zvaný natriuretický peptidový receptor typu B [NPR-B]. Čímž utlumí aktivitu FGFR3, stimuluje normální růst kostí a zlepšuje příznaky onemocnění [Ilustrace: BioMarin Pharmaceutical].
Účinek léčivého přípravku potvrdil Výbor pro humánní léčivé přípravky [CHMP] při EMA, a to na základě studie 121 pacientů s achondroplázií ve věku od pěti do 18 let. V ní se dosáhlo významného zlepšení růstu u pacientů léčených vosoritidem ve srovnání s placebem. Průměrná výška růstu pacientů dosáhla po roce léčby 1,57 cm. Zlepšení nastalo úměrně u páteře a dolních končetin.
Nejčastějšími vedlejšími účinky pozorovanými v klinických studiích byly hypotenze [nízký krevní tlak], reakce v místě vpichu a zvracení.
Možností léčby achondroplázie je více
Stanovisko přijaté výborem CHMP nyní dostala Evropská komise k přijetí rozhodnutí o registraci léku pro všechny unijní země. O ní zažádala irská společnost BioMarin International Limited. Látka je dostupná ve formě prášku i pro injekční podání.
Zabránit zvýšené aktivitě receptoru FGFR3, jehož nadměrná činnost zpomaluje růst buněk chrupavky u pacienta, čímž způsobuje onemocnění zvané achondroplázie, by v budoucnu mohl také RNA aptamer zvaný RBM-007. Ten dokáže fungovat jako past na ligandy, tedy malé proteiny, které vytvářejí komplexy s buněčnými receptory a dokáží aktivovat i již zmíněný receptor FGFR3. Právě kvůli jehož zvýšené aktivitě dochází ke zpomalení růstu. Studií léku zvaného RBM-007 se v Česku aktuálně zabývají vědci ve Fakultní nemocnici u sv. Anny [FNUSA-ICRC] a Biologickém ústavu LF Masarykovy univerzity v Brně.
Většina pacientů s touto nemocí je diagnostikována již v raném dětství nebo při narození. U některých se navíc často vyskytnou vážné zdravotní komplikace, jako jsou stlačení míchy, skloněné nohy, spánková apnoe, infekce uší, problémy se srdcem aj. Léčba byla doposud jen podpůrná ve smyslu chirurgických zákroků – prodloužení délky končetin, správné kompresi páteře nebo růstu nohou.
–DNA–